طیف نگاری کارکردی مادون قرمز نزدیک
fNIRS که روشی غیر تهاجمی است، میزان فعالیت مغز را تنها در محدوده چند میلیمتری از سطح کورتکس اندازه میگیرد و مبتنی بر تغییر در رنگ خون است هنگامی که اکسیژن به بافت مغز تحویل میگردد. (Villringer et al. 1993; Boas et al. 2004). fNIRS یک تکنولوژی پاسخ-قطعی(BOLD) است که تغییرات سطح نسبی اکسی- هموگلوبین و دی اکسی- هموگلوبین را در حین فعالیت مغزی اندازه میگیرد. خون سرشار از اکسیژن و حاوی اکسی-هموگلوبین بالا در سرخرگهای اصلی و سرخرگهای کوچکتر و همچنین بخشهای ابتدایی انشعاب مویرگهای مغز وجود دارد. خون دارای اکسیژن کم و حاوی دی اکسی-هموگلوبین بالا در بخشهای انتهایی مویرگها وجود داشته و درون سیاهرگها به سمت سیاهرگهای بزرگتر حرکت میکند که بزرگترین آنها بین دو نیمکره درست زیر جمجمه واقع شده است.
هنگامی که یک فرد مورد آزمایش کار خاصی را انجام میدهد، فعالیت مغزی در نواحی مرتبط با آن کار افزایش مییابد و میزان اکسی و دی اکسی- هموگلوبین در قسمتهای مجاور آن نواحی تغییر میکند. در حالت استراحت (قبل از اینکه شخص کاری انجام دهد)، یکسری فعالیت عصبی پایه و فعالیت متابولیک در حال انجام است و مقداری دی اکسی-هموگلوبین تولید میشود و بنابراین مقداری دی اکسی-هموگلوبین پایه وجود دارد. هنگامی که فعالیت ناحیه خاصی از مغز در حین انجام کاری افزایش مییابد، متابولیسم عصبی و گلیال هر دو افزایش مییابند. در ابتدا، همانطور که سلولها اکسیژن خون را میگیرند تا متابولیسم افزایش یافته مرتبط با فعالیت عصبی را پشتیبانی کنند، سطح دی اکسی- هموگلوبین افزایش مییابد. سپس سیستم عروقی سریعا برای جلوگیری از فقدان اکسیژن در نواحی پایین دست مغز دست به کار شده و خون غنی از اکسیژن را بسیار بیشتر از حد نیاز را فراهم میکند (Fox and Raichle1986). این موج ناگهانی خون تازه باعث میگردد که غلظت محلی اکسی-هموگلوبین افزایش یافته و غلظت محلی دی اکسی- همو گلوبین شدیدا افت کند (تقریبا تمام دی اکسی- هموگلوبین در نواحی مجاور از بین میرود). fNIRS از این حقیقت که مقدار نسبی اکسی –هموگلوبین و دی اکسی –هموگلوبین ناحیه تغییر میکند و این تغییر متناسب با سطح فعالیت عصبی است بهره میبرد. تغییرات در نسبت اکسی/ دی اکسی می توانند تشخیص داده شوند زیرا طیف جذب طول موجهای مادون قرمز نزدیک برای اکسی- هموگلوبین و دی اکسی- هموگلوبین متفاوتند (Boas et al. 2004). بدین صورت که:
- دی اکسی – هموگلوبین قرمز تیره است، نور با طول موج حدود 690 نانومتر را جذب میکند (به میزان بیشتری نسبت به آنچه اکسی- هموگلوبین جذب میکند)
- اکسی- هموگلوبین قرمز روشن است، نور با طول موج حدود 830 نانومتر را جذب میکند (به میزان بیشتری نسبت به آنچه دی اکسی- هموگلوبین جذب می کند)
در یک محیط همگن، تضعیف نور از قانون بیر-لمبرت پیروی میکند (Villringer and Chance 1997)، که بر اساس آن، تضعیف یا جذب ،A، متناسب با غلظت مولکول جاذب است:
![]()
که در آن غلظت مولکول جاذب، ضریب جذب آن (ویژگی برای یک ماده خاص) و عمق مسیر نوری است. تغییر در غلظت مولکول جذب، ، تغییر متناظری در جذب، ، ایجاد میکند بگونه ای که:
![]()
A میتواند توسط سنسور fNIRS در فواصل زمانی مختلف اندازهگیری شود، بنابراین قابل تعیین است. از آنجا که سر، یک محیط ناهمگن پیچیده برای مسیر عبور نور فراهم میکند، قانون بیر- لمبرت برای کاربردهای fNIRS اصلاح شده است (Villringer and Chance 1997) تا پارامترهای اضافی که اثرات پخش نور (مثل تضعیف سیگنال ناشی از دور شدن اشعهها از سنسور و افزایش طول مسیر ناشی از حرکت زیگزاگی اشعهها قبل از رسیدن به سنسور) را لحاظ میکنند را شامل شود. با این وجود، معادله بیر-لمبرت اصل اساسی زیربنایی اندازهگیری fNIRS از تغییرات در فعالیت مغزی را بیان میکند.
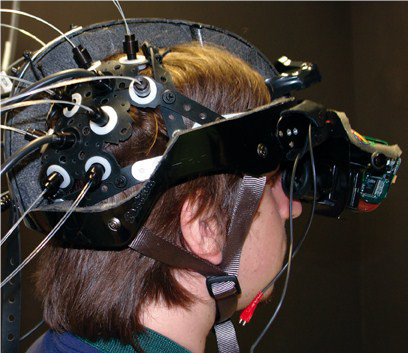
در fNIRS، نور با طول موجهای 690 و 830 نانومتر از طریق پروبهایی که روی پوست سر واقع شده اند به جمجمه تابیده میشود (شکل 1). این نور قادر است که از پوست و استخوان عبور کرده تا به بافت مغزی زیرین برسد. مقداری از نور توسط بافت مغزی جذب میشود. مقداری از نور پراکنده میشود، و بخشی از این نور پراکنده شده دوباره به درون سر بازتابیده میشود. بازتاب کم بدین معنی است که بیشتر آن جذب شده است. از آنجا که دی اکسی-هموگلوبین و اکسی –هموگلوبین الگوهای جذب متفاوتی در 690 و 830 نانومتر دارند، و چون جذب در یک طول موج مخصوص متناسب با غلظت مولکولهای جاذب است، اندازهگیری نور بازتابیده شده در طول موجهای 690 و 830 نانومتر به ترتیب غلظت مولکولهای جاذب، دی اکسی-هموگلوبین و اکسی – هموگلوبین را آشکار میکند. هنگامی که فعالیت مغز افزایش مییابد، غلظت دی اکسی-هموگلوبین ابتدا افزایش مییابد چون هموگلوبین خون اکسیژن خود را درون سلولها رها میکند. این یک اثر کوچک است و بصورت یک افزایش کوچک در جذب در 690 نانومتر (معرف دی اکسی-هموگلوبین بیشتر) آشکار میشود. بعد از جند ثانیه، جریان خون تازه حاوی اکسی-هموگلوبین در ناحیه مربوطه افزایش مییابد و بنابراین جذب در 830 نانومتر (معرف اکسی-هموگلوبین) افزایش مییابد. این یک اثر بسیار بزرگتر است زیرا عمدتا بدلیل افزایش بیش از حد جریان خون در ناحیه مورد نظر است (Fox and Raichle 1986).

شکل 1: مثالی از منابع و سنسورهای fNIRS. 4 لامپ ردیف وسط تابشکنندهها و در ردیف در لبهها آشکارسازها میباشند.
سخت افزار fNIRS
ابزارهای fNIRS شامل زوج منبع نور/آشکارساز (به همراه یکدیگر سنسور نامیده میشوند) میباشد که روی سر واقع شده است (شکل 1). بیش از حدود 52 زوج در حال حاضر امکانپذیر است که اندازهگیری بخش قابل توجهی از سطح مغز را فراهم میکنند. از آنجا که وجود مو مسیر نور را مسدود میکند (و جابجایی موها سیگنال را مختل میکند)، بهترین سیگنالها از قسمت پیشانی بدست میآیند. استفاده از سایر قسمتها نیز امکانپذیر است اما نیاز به جابجایی دقیق موهایی دارند که ممکن است منابع و آشکارسازها را مسدود کنند.
هنگامی که یک منبع نوری نور NIR را با یک طول موج مخصوص و تحت زاویه ای به درون جمجمه می تاباند، نور به درون مغز منتقل میشود، چند میلیمتر درون کورتکس نفوذ میکند و به بیرون سر بازتابیده میشود که در آنجا توسط آشکارسازهایی که در این مسیر واقع شدهاند آشکار میشود. انحراف فوتونها وقتی که از سطوح مشترک بین بافتهای مختلف عبور میکنند باعث میشود که یک مسیر منحنی شکل را از منبع تا آشکارساز طی کنند. این مسیر موز فوتون نامیده میشود (Hongo et al. 1995) و شکل آن به واسطه ویژگیهای اپتیکی بافتها تعیین میشود. اگر فاصله بین منبع و آشکارساز افزایش یابد و میزان جذب (به دلیل مسیر طولانی تر) نیز افزایش یابد، بیشتر موز از درون کورتکس عبور خواهد کرد. این اثر در شکل 2 نمایش داده شده است.
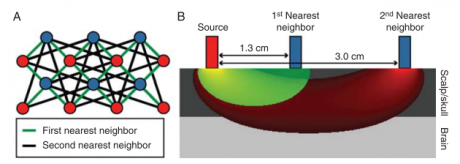
شکل 2: مثالی از طرح سنسورهای fNIRS
به هر حال، اگرچه افزایش فاصله منبع-آشکارساز میزان جذب را افزایش میدهد (بدلیل طول مسیر نوری بیشتر)، منجر به پراکندگی نور بیشتری نیز خواهد شد، که حساسیت fNIRS و رزولوشن مکانی را کاهش میدهد. در نتیجه، فاصله انتخابی مصالحهای بین این دو فاکتور متضاد است و باید برای کاربردی خاص مناسب باشد. از دادگان بدست آمده از آرایهای از سنسورهای fNIRS، نقشه ای از تغییرات همودینامیک میتواند ساخته شود که با عملکرد فعالیت مربوطه همبستگی دارد. این نقشه مشابه نقشههای fMRI است، اگرچه ناحیه تحت پوشش آن محدود است و رزولوشن مکانی آن بسیار کمتر است (شکل 3).
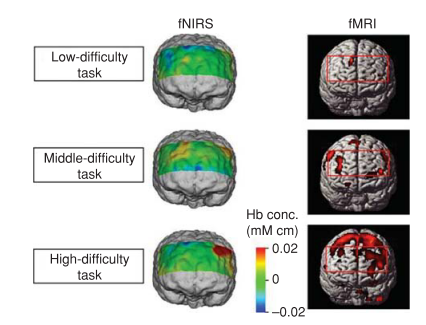
شکل 3: نقشههای فعالیت مغزی بدست آمده از fNIRS و fMRI با سه سطح دشواری از فعالیت مغزی
fNIRS روشی غیرتهاجمی، نسبتا ساده برای استفاده، قابل جابجایی و ارزان در مقایسه با سایر تکنولوژیهای اندازهگیری جریان خون است. رزولوشن زمانی آن نسبتا خوب (از مرتبه چند ثانیه)، اما رزولوشن مکانی آن نسبتا پایین (از مرتبه سانتی متر) است. این روش علیرغم محدودیتهایش، نوید دهنده ابزاری جهت توسعه BCI است.
BCI های مبتنی بر fNIRS
اصول روش شناسی fNIRS
همانگونه که پیش از این گفته شد، طیف نگاری مادون قرمز نزدیک مبتنی بر قانون بیر –لمبرت است که بیان میکند که تضعیف یا جذب نور در یک محیط همگن، A، متناسب با غلظت مولکول جذب است:
![]()
که در آن غلظت مولکول جاذب، ثابت تناسب است که ضریب جذب نامیده میشود و عمق مسیر نوری است. تغییر در غلظت مولکول جذب، ، تغییر متناظری در جذب، ، ایجاد میکند:
![]()
این تغییر با یک سنسور fNIRS آشکار میشود. همانطور که پیش از این گفته شد، fNIRS مبتنی بر این واقعیت است که نور مادون قرمز نزدیک (طول موجهای از 700 -1000 نانومتر، رنج مادون قرمز نزدیک [NIR] در طیف الکترومغناطیسی) در بافتهای زنده نفوذ میکند. این موضوع در زندگی روزمره نیز قابل مشاهده است، هنگامی که نور روشن به سمت کف دست باز تابیده میشود، نور از طریق بافت منتقل شده و منجر به تابش قرمزگونه ای در پشت دست میشود. این رنگ قرمز ناشی از رنگدانه هموگلوبین در خون است. چون مولکولهای آب و هموگلوبین نور NIR کمتری را نسبت به سایر طول موجها جذب میکنند، نور NIR (قرمز) از طریق بافت منتقل میشود.
هنگامی که زوج منابع نوری و آشکارسازها روی پوست سر قرار میگیرند، میتوانند انتقال NIR از طریق لایههای بافت مغز را اندازهگیری کنند. نوری که از بافت عبور میکند تحت تاثیر حالت عملکردی بافت قرار میگیرد. فعالیت مغزی با تغییراتی در مولفههای حاضر در خون (مثل تغییرات در غلظتهای هموگلوبین اکسیژندار شده و فاقد اکسیژن شده (Villringer and Obrig, 2002)) همراه است. این تغییرات میتوانند بصورت تغییراتی در سیگنال fNIR بعد از عبور نور مادون قرمز نزدیک از بافت مغزی آشکار شوند. در نتیجه، اندازهگیری fNIRS آشکارسازی و اندازهگیری غیر مستقیم فعالیت مغزی را سبب میشود.
اگرچه رزولوشن مکانی سیگنال fNIRS (در رنج سانتی متر) کمتر از مقدار مشابه در تصویربرداری تشدید مغناطیسی کارکردی (fMRI) (در رنج میلی متر) است، fNIRS مزایای قابل توجهی نسبت به سایر روشهای تصویربرداری مغز دارد. نخست اینکه fNIRS ایمن و غیرتهاجمی است. این روش از تشعشات بالقوه مضر استفاده نمیکند زیرا نور مادون قرمز نزدیک غیریونیزه شده را بکار میبرد. شدت نور پایینتر از محدوده امن نگه داشته میشود تا از آسیبهای دمایی اجتناب شود. fNIRS به تزریق مواد کنتراست احتیاج ندارد. با fNIRS، تابع بافت به تنهایی سیگنالی را تولید میکند که تصویر میشود. fNIRS تغییرات در غلظت هموگلوبین و تغییرات در اکسیژن اشباع بافت را کنترل میکند و میتواند از روی این مقادیر، پرفیوژن بافت و عرضه/تقاضای اکسیژن را محاسبه کند. با پیشرفتهای اخیر در میکروالکترونیک، مهندسی اپتیک، و تکنولوژی کامپیوتر، سیستمهای fNIRS میتوانند نسبتا کوچک، بسادگی قابل حمل (بویژه در مقایسه با سیستمهای fMRI)، و بسیار ارزانتر از سایر روشهای تصویربرداری مثل fMRI و مقطع نگاری با انتشار پوزیترون (PET) شوند.
در یک اندازهگیری fNIRS معمول از فعالیت بافت مغزی، یک دیود نوری (که اپتود (optod) نامیده میشود) بصورت یک منبع نور (یا متشر کننده) عمل میکند. نور ساطع شده توسط اپتود از لایههای واسط پوست سر و جمجمه عبور کرده، وارد بافت غشایی شده، و سپس از طریق پوست سر و جمجمه به یک یا چند آشکارساز واقع شده در فواصل ثابت از منبع بازگردانده میشود. آشکارساز معمولا یک اپتود دریافت کننده نور است که متصل به یک ضرب کننده نوری یا یک ابزار متصل به شارژ (CCD) میباشد.
در تشریح اینکه fNIRS چطور تغییرات در فعالیت مغزی را آشکار میکند، ابتدا باید دو تغییر فیزیولوژیکی که همراه با تغییرات در فعالیت مغزی است را مرور کنیم. این تغییرات مسئول آن چیزی هستند که پاسخ قطعی (bold) نامیده میشود. به اختصار، جریان خون مغزی محلی (rCBF) و نرخ متابولیک اکسیژن مغزی محلی (rCMRO2) هر دو به هنگام افزایش فعالیت مغزی در آن محل افزایش مییابند. در هر حال، افزایش در rCBF بیشتر از افزایش در rCMRO2 است، بدین معنا که افزایش rCBF بیشتر از افزایش مورد نیاز برای تامین اکسیژن اضافی مورد نیاز است (Raichle,1986 Fox and). در نتیجه، اگرچه غلظت هموگلوبین و غلظت اکسی-هموگلوبین (oxy-Hb) هنگام فعالیت مغزی افزایش مییابد، غلظت دی اکسی-هموگلوبین (deoxy-Hb) کاهش مییابد. از آنجا که oxy-Hb و deoxy-Hb نور را در طول موجهای مادون قرمز نزدیک متفاوتی جذب میکنند، fNIRS میتواند تغییرات غلظتهای نسبی آنها را با اندازهگیری تغییرات تضعیف نور در فرکانسهای مشخصی آشکار کرده و سپس پاسخ قطعی را محاسبه نماید که مرتبط با تغییرات همزمان در فعالیت عصبی است.
سه نوع طیف نگاری اساسی مورد استفاده در fNIRS عبارتند از: طیف نگاری موج-پیوسته، طیف نگاری زمان- ثابت و طیف نگاری حوزه فرکانس. این تکنیکها با جزئیات در Villringer and Obrig, 2002)) توضیح داده شدهاند. رویکرد موج-پیوسته (CW) همان روشی است که بطور گستردهای در تصویربرداری عصبی و مطالعات BCI استفاده میشود. در ابزارهای CW fNIRS تجاری موجود، منبع نور یا یک لیزر است، یا دیود نوری (LED)، یا یک لامپ هالوژن ساده که نور را در فرکانسهای مشخصی در محدوده طیف NIR میتاباند. از مزایای رویکرد CW سادگی، انعطاف پذیری، و قابلیت دستیابی به نسبت سیگنال به نویز بالا را میتوان نام برد. یکی از معایب این روش این است که رویکرد CW نمیتواند کمیت مقادیر مطلق اکسی-هموگلوبین و دی اکسی-هموگلوبین را تعیین کند و تنها تغییرات نسبی آنها را نشان میدهد. عیب دیگر این روش این است که مقادیر اندازهگیری شده آن نسبت به اعوجاج در تغییرات جذب نور در بافتهای سطح خارجی مغز مثل پوست سر حساس هستند.
در اغلب کاربردهای fNIRS، از جمله کاربرد در BCI، هدف اولیه از آنالیز داده آشکارسازی تفاوتهای فعالیتهای مغزی در نواحی مشخص بصورت تابعی ازحالات رفتاری مختلف است. بعنوان مثال، ممکن است هدف آشکارسازی تفاوت فعالیت مغزی در دو حالت استراحت و انجام حرکتی مشخص باشد. بطور خاص در کاربرد BCI، هدف میتواند آشکارسازی تفاوتهای فعالیت مغزی بین دو حالت یک فعالیت باشد: وقتی شخص میخواهد یک اشاره گر را به سمت چپ حرکت دهد در مقایسه با وقتی که میخواهد آن را به سمت راست حرکت دهد.
ساختار و عملکرد fNIR-BCI
مشابه تمامی سیستمهای BCI، یک سیستم fNIR-BCI مولفههایی برای جمع آوری و همچنین پردازش سیگنال (استخراج ویژگی و انتقال) دارد. این سیستم یک خروجی تولید میکند که دستوری به یک برنامه کاربردی صادر میکند و بازخوردی زمان-واقعی بسته به نوع کاربرد را برای کاربر فراهم میکند. این مولفه ها در شکل زیر نشان داده شده اند.
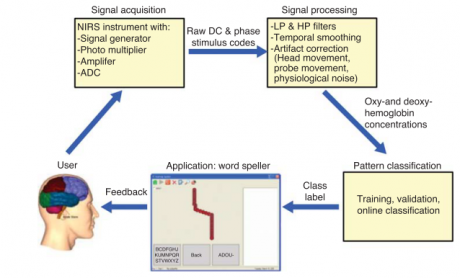
شکل 4: معماری پایه یک BCI مبتنی بر fNIRS
اکتساب (جمع آوری) سیگنال fNIR
شکل 5 المانهای اساسی یک سیستم اندازهگیری fNIRS را تشریح میکند. این المانها شامل: ساطع کننده نور (بعنوان منبع یا نورافکن نیز شناخته میشود)؛ یک آشکارساز؛ یک تقویت کننده؛ یک مبدل آنالوگ به دیجیتال؛ و در نهایت سیگنالهای fNIR قابل استفاده بصورت بالقوه میباشند. اپتودهای تابش کننده (قرمز) و آشکارساز (آبی) در محلهای متناوب مشخصی روی پوست سر واقع شده اند (شکل 5-ب). فاصله بین تابش کننده و آشکارساز در هر زوج تابش/آشکارساز بسته به آرایش آنها روی پوست سر در محدوده 30-5 میلیمتر است. یک زوج تابش/ آشکارساز بعنوان یک کانال در نظر گرفته میشود.
شکل 5-ب مثالی از یک پیکربندی اپتود است که در آن اپتودهای تابش کننده (قرمز) و آشکارساز (آبی) روی پوست سر در موتور کورتکسهای چپ و راست واقع شدهاند (یعنی نزدیک مکانهای C3 و C4 [سیستم 20-10 بین المللی]). اپتودهای آشکارساز در فاصله 2 سانتی متر از اپتودهای تابش کننده واقع شدهاند. همانطور که با خط چین در شکل 5-ب نشان داده شده است، هر زوج اپتود تابش کننده/آشکارساز یک کانال را تشکیل میدهند. در نتیجه، با چهار تابش کننده و چهار آشکارساز، پیکربندی اپتود نشان داده شده در شکل، 10 کانال برای هر نیمکره را نتیجه میدهد. همانطور که در شکل شکل 5-الف نشان داده شده است، اشعه های مادون قرمز نزدیک از هر تابش کننده ساطع شده و از درون جمجمه و بافت مغزی کورتکس عبور کرده و یک مسیر منحنی شکل تعیین شده توسط ویژگیهای اپتیکی بافت را طی کرده و به جمجمه بازتابیده میشود، و توسط یک یا چند اپتود آشکارساز دریافت میشود (موز فوتونی قرمز مسیر فوتونها را نمایش میدهد). ضرب کننده نوری در همه زوجهای تابش کننده-آشکارساز میگردد تا داده ها را در هر تناوب نمونه برداری جمع آوری کند.
بعد از اینکه سیگنالها در هر فرکانس جمع آوری و دیجیتالی شدند، پیش پردازش میشوند (برای مثال آرتیفکتها حذف میشوند)، سپس بیشتر پردازش میشوند تا غلظتهای اکسی-هموگلوبین و دی اکسی-هموگلوبین استخراج شوند، و در نهایت روی هارد دیسک ایستگاه کاری fNIRS-BCI ذخیره میشوند. در هر نقطه زمانی، فایل ذخیره شده معمولا شامل: شدتهای سیگنال خام برای هر یک از دو یا سه طول موج استفاده شده؛ تغییرات غلظت Hb محاسبه شده از روی این شدتها؛ و و کدهایی که بر حالت رفتاری فعلی شخص دلالت میکنند (مثل تصور حرکت دست راست، نگاه کرردن به نشانه روی یک صفحه و …) میباشد. اگر سیستم در حالت زمان-واقعی کار کند که یک عملکرد را کنترل کرده و بازخورد را برای شخص فراهم کند، دادگان بطور همزمان تحت پردازش اضافی جهت تولید سیگنالهای فیدبک خروجی نیز هستند. چنین کاربرد زمان-واقعی معمولا یک پروسه کالیبراسیون اولیه (و احتمالا کالیبراسیونهای مجدد دورهای) را نیز شامل میشود تا پارامترهایی که برای تبدیل اندازه های غلظت اکسی-هموگلوبین و دی اکسی-هموگلوبین به مقادیر خروجی استفاده میشوند را تعریف کنند.
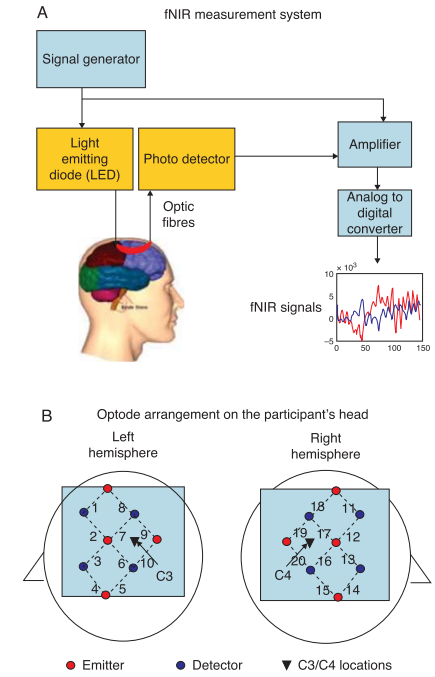
شکل 5: سیستم اندازهگیری fNIRS
موفق باشید.
نویسنده: ملیحه میری


دیدگاه ها