تصویربرداری FMRI
در جلسات قبل درباره ی ثبت های مغزی و همچنین روش های تصویربرداری جریان خون بحث کردیم. در این جلسه در مودر تصویربرداری FMRI صحبت خواهیم کرد.
دستگاه گردش خون یکی از دستگاههای بدن است که کارش به گردش درآوردن خون در بدن به منظور رساندن غذا (آمینواسید، الکترولیت، لنف)، انواع گازهای مورد مصرف بدن همچون اکسیژن و دفع مواد زاید حاصل از متابولیسم سلول هاست. بطور کلی، چرخش خون در بدن به دو چرخه (گردش) ششی، که در حین آن خون توسط قلب به درون ششها هدایت شده و در آنجا اکسیژن دریافت میکند، و چرخه سیستمیک (کل بدن منهای بخش گازی ریه)، که در حین این چرخه خون توسط قلب به کل بدن هدایت شده و اکسیژن و مواد غذایی را به کل سلولهای بدن میرساند.
یکی از وظایف کلیدی خون، حمل اکسیژن می باشد. قلب خون اکسیژن دار را از طریق شریانها به کوچکترین رگ های خونی، مویرگ پمپاژ کرده و از از طریق مویرگها خون به اندامها و عضلات می رسد و در آنجا اکسیژن رها می شود، که تامین کننده فرایند متابولیکی است. و دی اکسید کربن تولید شده توسط فرایندهای متابولیکی را جذب می کند. و از طریق عروق خونی به قلب رسیده و قلب خون دی اکسید کربن دار را به ریه ها انتقال می دهد و در ریه خون دی اکسید کربن را رها کرده و به جای آنها اکسیژن جذب می کند، خون اکسیژن دارشده دوباره به قلب انتقال می یابد و این چرخه ادامه پیدا میکند.
هرچرخه حدودا یک دقیقه طول می کشد. در داخل خون، حمل اکسیژن توسط هموگلوبین انجام میشود.
هموگلوبین به علت داشتن آهن که در حالت احیا شده میباشد، میتواند با اکسیژن و دیاکسید کربن ترکیب شده و به ترتیب اکسی هموگلوبین (oxyhemoglobin) و کربو آمینو هموگلوبین (carbaminohemoglobin (دی اکسی هموگلوبین ) تشکیل دهد. با توجه به بالابودن فشار اکسیژن در ریهها ، اکسی هموگلوبین در ریهها تشکیل شده و پس از رسیدن به بافتها ، اکسیژن جدا شده و دیاکسید کربن CO2 به آن متصل میگردد. به این ترتیب امکان حمل اکسیژن از ریهها به بافتها و دیاکسیدکربن از بافتها به ریهها امکانپذیر میگردد. از طرف دیگر سطح بسیار زیاد گویچههای قرمز نسبت به حجم آنها (به علت داشتن شکل مقعرالطرفین) سبب تسریع و تسهیل اشباع هموگلوبین با اکسیژن در ریهها میشود. علاوه بر انتقال اکسیژن توسط هموگلوبین ، این مولکول عمل دیگری نیز انجام میدهد و آن عبارت از تثبیت فشار اکسیژن در بافتها است.
زمانی که فعالیت متابولیکی یک ناحیه ای از مغز افزایش می یابد، مصرف اکسیژن آن بالا می رود، بعد از حدود ثانیه و یا بیشتر، نورونها شروع به جذب اکسیژن بیشتری از اکسی هموگلوبین موجود در خون می کند (اینکه در این گپ زمانی (تاخیر) چه اتفاقی می افتد هنوز مشخص نشده است). تخمین زده شده است که مصرف اکسیژن توسط نورون 80 درصد از مصرف انرژی در بافت مغزی را شامل می شود. در مقابل سلولهای گلیال حدود 5 درصد انرژی را مصرف می کنند و به همین دلیل تقاضای متابولیکی کمتری دارند. مویرگها در پاسخ به تقاضای اکسیژن توسط نورونها، گشاده شده و باعث می شوند که خون زیاد و تازه ای وارد ناحیه فعال مغزی شود.
در این فرایند، سه تغییر مهم اتفاق می افتد:
- مقدار خون در ناحیه فعال مغز افزایش می یابد
- فشار خون افزایش می یابد
- اکسی هموگلوبینها اکسیژن را رها کرده و تبدیل به دی اکسی هموگلوبین می شوند.
زمانی که فعالیت ناحیه مغزی به حالت نرمال خود باز میگردد، این سه رویداد به حالت اولیه خود باز می گردند.
در ادامه دو روش اساسی تصویربرداری جریان خون در مغز، fMRI، و fNIRS که نسبت به چهار روش قبلی کاربرد بیشتری در BCI دارند، توضیح داده خواهد شد.
fNIRS اختلاف رنگها در دی اکسی هموگلبین و اکس هموگلبوبین را اندازه گیری می کند و fMRI اختلاف در خواص مغناطیسی دی اکسی هموگلبین و اکس هموگلبوبین را اندازه گیری می کند.
- اکسی هموگلوبین، قرمز روشن و دی اکس هموگلوبین قرمز تیره است.
- oxy-Hb غیر مغناطیسی (“diamagnetic”) است، در حالی که deoxy-Hb کمی مغناطیسی (“paramagnetic”) است
به طور خاص، fNIRS ، زمانی که oxy-Hb به deoxy-Hb تبدیل می شود ، تغییر در جذب مادون قرمز نزدیک را اندازه گیری می کند، در حالی که fMRI تغییرات خواص مغناطیسی، تغییر مقدار نسبی اکسی Hb و دیاکسی Hb در طول فعالیت مغز، را اندازه گیری می کند.
فعالیت مغز شامل برقراری ارتباط میان میلیونها نورون است. از آنجایی که یک ارتباط خاص که شامل فرستنده و گیرنده (اغلب در قسمت های مختلف مغز قرار دارند) است، مهم است بدانیم که آیا تغییرات همودینامیکی برای فرستنده و گیرنده هم یکسان است یا اینکه آیا متفاوت هست. اندازه گیری ارتباطات به طور مستقیم امکان پذیر نیست زیرا هر نورون به هزاران نورون دیگر متصل است، و باعث میشود یک سیستم بسیار پیچیده ای را تشکیل دهد (Buzsaki 2006). تغییرات در ارتباطات را می توان به صورت غیر مستقیم توسط اندازه گیری نرخ شلیک (firing rate) تک نورون یا پتانسیل های محلی (LFPs) ، و یا با اندازه گیری پتانسیلهای میدان بزرگ توسط ECoG و یا EEG انجام داد. تغییرات ارتباطات را میتوان با استفاده از fNIRS یا تصویربرداری fMRI از طریق اندازه گیری تغییرات همودینامیکی مرتبط با ارتباط را نیز انجام داد.
تصویربرداری تشدید مغناطیسی کارکردی (Functional Magnetic Resonance Imaging-fMRI)
این روش در سال 1990 به عنوان یک روش تصویربردای مفید ظهور کرد، و بعد از آن با سرعت بالایی توسعه پیدا کرد. این روش رزولوشن مکانی خیلی خوبی دارد و امروزه یکی از رایجترین روشها برای تصویربرداری عملکردی مغزی می باشد. این روش نیز برپایه bold-response میباشد و مقادیر مرتبط دی اکسی و اکسی hb در بافت مغز را اندازهگیری می کند. این ایده که جریان خون مغزی(CBF)میتواند فعالیتهای عصبی را منعکس کند با آزمایشهای Roy وSherrington در سال ۱۸۹۰ شروع شد. این مفهوم پایه تمام تکنیکهای تصویربرداری امروزی است که براساس همودینامیک از مغز انجام میشود. تغییرات جریان خون و میزان اکسیژن خون مغز (همراه با هم همودینامیک نامیده میشوند) که به خوبی با فعالیتهای عصبی مرتبط هستند. افزایش محلی CBF میتواند مستقیماً مرتبط با فعالیت الکتریکی باشد، زیرا متابولیسم گلوکز و تغییرات CBF به خوبی کوپل هستند.[۳] بنابراین، اندازهگیری تغییرات CBF ایجاد شده توسط یک محرک میتواند برای نگاشتن عملکرد مغز استفاده شود. از آنجاییکه نرخ متابولیک مغزی گلوکز (CMRglu) و تغییرات CBF کوپل هستند، به نظر میرسد نرخ متابولیک مغزی اکسیژن (CMRO2) و تغییرات CBF نیز کوپل هستند. بر اساس اندازهگیریهای CBF و CMRO2 توسط PET نشان داده شد که میزان افزایش در افزایش CBF به میزان افزایش در CMRO2 برتری دارد. در نتیجه، یک عدم تطبیق بین تغییرات CMRO2 و CBF باعث افزایش سطح اکسیژن خون در سرخرگها و سیاهرگها میشود، که یک پارامتر جدید را (علاوه بر CBF) برای نگاشتن فعالیتهای مغز معرفی میکند. BOLD یک کنتراست MRI از دی اکسی هموگلوبین خون است؛ که برای اولین بار توسط Ogawa و همکارانش در آزمایشگاه Bell دانشگاه AT&T در سال ۱۹۹۰ کشف شد. کنتراست BOLD وابسته به تغییرات دی اکسی هموگلوبین(dHb) خون است، که به عنوان یک ماده کنتراست پارامغناطیس درونی عمل میکند؛ بنابراین، تغییر در میزان غلظت dHb محلی در مغز نمایندهای از میزان شدت سیگنال MRI خوهد بود. روش تصویربرداری BOLD به دلیل حساسیت بالا و اجرای ساده آن بهطور وسیعی استفاده میشود. اما سیگنال BOLD به پارامترهای آناتومیکی، فیزیولوژیکی و تصویربرداری وابسته است و تفسیر آن با توجه به پارامترهای فیزیولوژیک به صورت کیفی و نیمه کمی است؛ بنابراین، مقایسه نتایج ازمایشگاههای مختلف با میدانهای مغناطیسی مختلف، با هم مشکل است. در مقابل تغییرات CBF نیز توسط MRI قابل اندازهگیری است و چون سیگنالهای fMRI وابسته به یک پارامتر فیزیولوزیک است، تفسیر کمی آن سر راست تر است.
قبل از اینکه نحوه تصویربرداری fMRI و کاربرد آن در BCI را توضیح دهیم، لازم است که خواص اسکنرهای MRI و اصول تصویربردای آن را توضیح دهیم.
اجزای دستگاه MRI
یک دستگاه MRI از 6 عنصر اصلی تشکیل شده است:
- یک آهنربای بزرگ (a large main magnet)
- یک فرستنده رادیوفرکانسی(a radiofrequency transmitter)
- یک آنتن گیرنده(a receiver antenna)
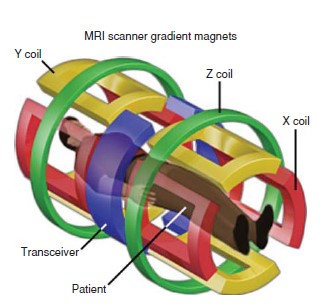
- کویل های گرادیان(gradient coils)
- یک کامپیوتر جلویی(a front-end computer)
- یک کامپیوتر بازسازی(a reconstruction computer)
– آهنربای بزرگ (large main magnet)
آهنربای بزرگ از یک ورقه(تونل) آلومنیمی با طول 2 متر و عرض 1 متر تشکیل شده است که نسبت به مرکز خود چرخش می یابد.
سیمها اطراف تونل پیچیده شده اند تا چندین حلقه سیمی را تشکیل دهند. آهنربا MRI از سیم مسی استاندارد استفاده نمی کند زیرا جریانهای الکتریکی بالا برای تولید میدان مغناطیسی بالای مورد نیاز جهت تصویربرداری باعث می شود که خنک کردن سیم های مسی سخت شود و در نتیجه مقاومت سیم مسی افزایش یابد و از این طریق مانع ایجاد میدان مغناطیسی بالا شود. به جای استفاده از سیم مسی، از سیمهای ابرسانا که ترکیب نایوبیتیتیونیوم و مس است، استفاده می کنند. این مواد ابرسانا در دماهای پایین مقاومت صفر در برابر جریانهای الکتریکی دارند. در داخل آهنربا، سیم در یک پوشش آلومینیومی قرار دارند که حاوی هلیوم مایع نگهداری شده در 269 درجه سانتیگراد (4 کلوین) می باشد. در این دما سیمها تبدیل به ابررسانا می شوند. که این امکان را فراهم می کند که جریانهای بالا جهت ایجاد میدان مغناطیسی بالا برای تصویر برداری از سیمها عبور کنند. میدان مغناطیسی تولید شده را میدان B0 می نامند. قویترین میدانی که در حال حاضر تولید میکنند بیشتر از 20 تسلا است. هرچقدر این میدان قوی باشد، شدت روشنایی تصاویر بهتر خواهد بود. به خاطر اینکه یک تونل جهت قرار گرفتن انسان در داخل آن ایجاد میوشد، امکان تولید میدان های قوی تر سخت است، و قویترین میدانی که دستگاهای MRI جهت تصویربردای از انسان استفاده می کنند حدود 11.7 تسلا است. اکثر بیمارستانها جهت انجام کاراهای تشخیصی و تحقیقاتی از MRI 3 تسلا استفاده می کنند.

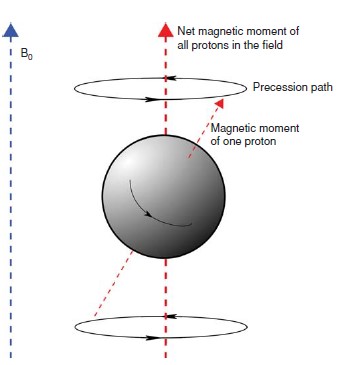
بافت بدن انسان به خودی خود میدان مغناطیسی ندارد. اما غنی از هیدروژن است. هسته یک اتم هیدروژن(پروتون) یک اسپین ذاتی دارد که یک میدان مغناطیسی کوچکی اطراف هسته و یک گشتاور زاویهای تولید می کند. همانطور که با یک خط قرمز رنگ در شکل نشان داده شده است.
میدانهای کوچک تولید شده توسط پروتونهایی که هر کدام در جهات مختلفی(تصادفی) هستند، توسط یکدیگر خنثی می شوند. با توجه به اینکه هسته هیدروژن دارای حرکت و بار مثبت است. پس طبق قانون القاء فارادی بهطور خود به خود یک گشتاور مغناطیسی پیدا میکنند؛ و با قرار گرفتن در یک میدان مغناطیسی خارجی مرتب میشوند. برخی هستههای اتم هیدروژن با میدان هم راستا میشوند، و تعداد کمتری از هستهها پاد موازی با میدان مغناطیسی هم راستا میشوند. تأثیر میدان مغناطیسی خارجی ایجاد یک نوسان اضافی برای هستههای هیدروژن حول خود میدان است که این حرکت را، حرکت تقدیمی مینامند.
 – فرستنده و آنتن گیرنده رادیوفرکانسی:
– فرستنده و آنتن گیرنده رادیوفرکانسی:
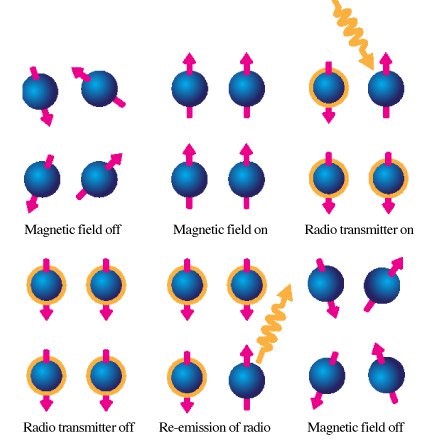
فرستنده رادیوفرکانس دومین عنصر اصلی دستگاه MRI است، این فرستنده پالسهای رادیوفرکانسی به سر شخص می فرستد.
بعد از آنکه میدان مغناطیسی قوی تولید شد و پروتونها را در یک راستا قرار داد، برای آنکه تشدید هستههای هیدروژن رخ دهد، یک پالس RF با همان فرکانس حرکت تقدیمی به کار میرود. اعمال پالس RF که سبب تشدید هستهها میشود، را تحریک مینامند. در نتیجه این تشدید هستههای هیدروژن هم راستا با میدان مغناطیسی خارجی باقی نمیماند. به زاویهای که بین هستههای هیدروژن و میدان مغناطیسی خارجی ایجاد میشود، زاویه فلیپ FA میگویند. اگر این زاویه ۹۰ درجه باشد بیشترین مقدار انرژی به کویلهای گیرنده القاء میشود. طبق قانون القاء فارادی اگر یک کویل گیرنده در صفحه حرکت این میدان مغناطیسی قرار گیرد، ولتاژ در کویل القاء میشود. وقتی میدان مغناطیسی عرض صفحه کویل را قطع کند، سیگنال MR تولید میشود. این سیگنالها که در زمان Relaxation پروتونها تولید می شوند، توسط گیرنده های رادیوفرکانسی دریافت می شوند. در شکل روبرو فرایند ایجاد سیگنال mr نشان داده شده است.
– کویلهای گرادیان (gradient coils):
برای شناسایی مناطق مغزی مرتبط با سیگنالهای خاص، کامپیوتر بازسازی تصویر نیاز دارد که منشاء فضایی سیگنالهای تشخیص داده شده را تفیکیک کند. این اطلاعات توسط کویلهای گرادیان فراهم می شود. کویلهای گرادیان شامل آهنرباهای اضافی است که داخل آهنربای اصلی قرار داده شده اند. آهنربای کویلهای گرادیان در مقایسه با آهنربای اصلی ضعیف هستند، اما زمانی که به میدان B0 اضافه می شوند، میتوانند میدانهای مغناطیسی گرادیان در میان بافت تصویر برداری شده تولید کنند. در یک دستگاه MRI، زمانی که آهنرباهای گرادیان فعال می شوند، به خاطر ترکیب اثر میدان B0 و کویلهای گرادیان، بخشهای مختلف مغز، شدت میدان مغناطیسی متفاوتی تجربه می کنند. به خاطر شدت میدان مغناطیسی متفاوت، فرکانس های لارمور متفاوتی ایجاد می کنند، پروتونها در مکانهای مختلف مغز، سیگنال RF متفاوتی جذب خواهند کرد، سپس سیگنالهای RF با فرکانس رزونانس(لارمور) دقیقا متناظر با میدان محلی خود منتشر می کنند.
– کامپیوتر جلویی و کامپیوتر بازسازی تصویر
کامپیوتر جلویی دنباله پالس را کنترل می کند، پالسهای که دنباله های پیچیده ای دارند، و ترکیب پالسهای RF و کویل گرادیان می باشند.
دنباله های پالسی مختلفی وجود دارد که هر کدام تصاویر مختلفی از قبیل تصویر آناتومی، جریان خون، تشخیص تومور و غیره ایجاد میکنند. برای fMRI، فقط چند توالی از پالسها مورد استفاده قرار می گیرند، و یکی از پالسهایی که به طور وسیع استفاده می شود، تصویربرداری echo-planar نامیده می شود. دنباله های پالسی نه تنها میدان های گرادیان تولید می کنند، همچنین زمان relaxationهای پروتونها در موقعیتهای مختلف را تحت تاثیر قرار می دهد. کامپیوتر باسازی با استفاده از این اطلاعات درباره توزیع دقیق میدانهای مغناطیسی و مشخصات relaxations پروتونها، سیگنالهای خاص را به موقعیتهای خاص مغز ارتباط می دهد.
اندازه گیری fmri از BOLD response
روش Fmri، نقشه ای از پاسخ همودینامیک فعالیت مغز را براساس اثری که دی اکسی Hb روی میدان مغناطیسی دارد، تولید می کند. همانطور که قبلا اشاره کردیم، اثر همودینامیک باعث تولید سیگنالهای boldی می شود که برای اولین بار توسط Oqawa و همکارانش توصیف شد. اصل کلیدی این است که دی اکسی Hb یک اختلاف اضافی در میدان مغناطیسی تولید شده توسط آهنربای اصلی و کویلهای گرادیان می شود. دی اکسی Hb قدرت میدان مغناطیسی در منطقه نزدیک خود را تغییر می دهد، به همین خاطر قدرت میدان محلی واقعی کمی پایین تر از میدانی است که توسط توالی پالس پیش بینی می شود. این کاهش، به خاطر وجود دی اکسی Hb، به عنوان یک نقطه تاریک کوچک در تصویر ساخته شده آشکار می شود. شدت روشنایی نقطه تاریک با مقدار دی اکسی Hb موجود ارتباط دارد. .
از آنجا که تصویربردای fMRI بسیار سریع است، تنها چند ثانیه طول می کشد تا یک تصویر از کل مغز تولید کند، می توان یک مجموعه ای از تصاویر(یک فیلم) براساس مقدار دی اکسی Hb در موقعیتهای خاص مغز در طول زمان تولید کرد.
همانطور که قبلا توضیح دادیم، فعالیت مغز باعث تغییرات در میزان دی اکسی Hb و اکسی Hb می شود. در ابتدا، زمانی که اکسیژن به سلولها رها می شود، دی اکسی افزایش می یابد، و این باعث تیره شدن بخش فعال مغز میشود. سپس زمانی که عروق خونی به نیاز سلول جهت اکسیژن رسانی پاسخ می دهند، افزایش جریان خون باعث کاهش غلظت دی اکسی Hb شده و در نتیجه بخش فعال مغز در تصویر روشن تر می شود. از اینرو در هنگام شروع فعالیت مغز، تصویر در ابتدا تیره شده و سپس روشنتر می شود. افزایش روشنایی متناظر با میزان فعالیت مغز است. بنابراین، نقشه های مغزی را میتوان براساس تغییرات در میزان تغییرات روشنایی در تصاویر fMRI ایجاد کرد.
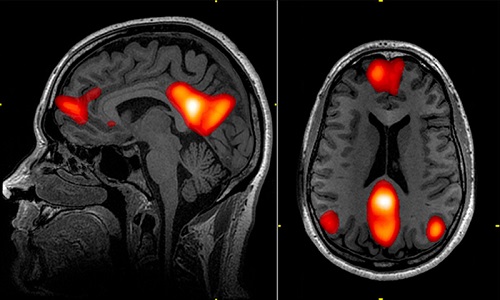
مجموعه ای از چنین نقشه هایی در شکل پایین نمایش داده شده است. در این روش، تصاویر fMRI می توانند مناطق مغزی که در طول انجام وظایف مشخص (specific task) فعال بودند، را آشکار کنند.
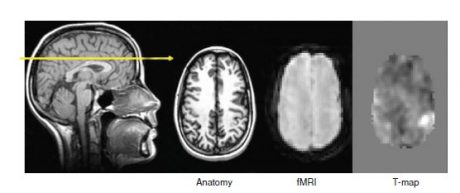
تصویربرداری نورونی عملکردی موثر با استفاده از fMRI نیاز به اسکنهای زیادی دارد، زیرا که اثر BOLD کوچک است، و به خاطر حرکات سر، تنفس، پالسهای عروق خونی، نویزهای قابل توجهی به تصاویر اضافه می شود. نرم افزارهای مختلفی برای تحلیل تصاویر fMRI موجود است. این نرم افزارها الگوریتمهایی دارند که اثر نویز را کاهش می دهند.
نرم افزارهایی که به طور گسترده استفاده می شوند عبارت اند از :
- SPM ( https://www.fi l.ion.ucl.ac.uk/spm/ )
- AFNI ( https://afni.nimh.nih.gov/afni )
- FSL( https://www.fmrib.ox.ac.uk/fsl/ )
- و برنامه تجاری Brainvoyager ( https://www.brainvoyager.com/)
تمام این برنامه ها نقشه های مغزی را براساس معیارهای آماری از قبیل t,F ایجاد می کنند. در یک t-map، هر وکس یک مقداری دارد که نشان دهنده میزان تغییر سیگنال در ارتباط با کار انجام شده در طول اسکن است. مقدار t بالا به این معنی است که تغییرات فعالیت مغز برجسته تر از نویز است.
طراحی تسک(task) برای تصویربرداری عصبی عملکردی
همه تکنیکهایی که توضیح داده شد، تصاویر عملکردی از مغز تولید میکنند. تصویری که نقشه ها ارائه میدهند به تسکی که subject در طول تصویربرداری انجام می دهد بستگی دارد. بنابراین، تسکهای آزمایشی برای آشکارسازی بخشهای خاص مغز که عملکردهای خاصی را انجام میدهند، طراحی می شود.
هدف اصلی تصویربرداری عصبی عملکردی این است که نشان دهد بخشهای مختلف مغز مسئول چه عملکردی هستند. برای مثال، در هنگام خواندن کتاب، تنها بخش مربوط به شبکه زبان فعال نیست، بخشهای دیگری از قبیل سیستم بینایی، سیستم حافظه، و حتی سیستم حرکتی نیز جهت خواندن، درک و تفسیر متن، حرکت دادن چشم به سمت جلو و عقب فعال هستند. فرض کنید که ما میخواهیم یاد بگیریم که کدام بخشهای مغز در زبان درگیر هستند، برای این منظور ما هنگامی شخص یک متنی را از صفحه میخواند، تصاویر fmri را ثبت می کنیم، هرچند این تصاویر به تنهایی اطلاعات مهمی به ما نمی دهند، زیرا که مغز همیشه در حالت فعال است، حتی در زمان خواب و بیهوشی مغز فعال است! زمانی که فرد یک تسک خاصی را انجام می دهد، بخشهای زیادی از مغز ممکن است درگیر باشند. چیزی که نیاز است این است که ما تغییراتی که در زمان خواندن متن در تصویر ایجاد می شوند را پیدا کنیم. اینکار با استفاده از طراحی تسکهای خاص برای subject انجام میشود، البته با استفاده از یک سری نرم افزارهای خاصی مثل “presentation” انجام می شود. برای مثال، در زمان تصویربرداری، subject باید در ابتدا به یک صفحه سفید به مدت 30 ثانیه نگاه کند، سپس متن را به مدت 30 ثانیه بخواند، و بعد از خواندن متن، دوباره به یک صفحه سفید نگاه کند. این چرخه باید چندین بار تکرار شود، سپس تجزیه و تحلیلهای بعدی در هر وکسل کورولیشن(همبستگی) بین تسکها( خواندن متن در مقابل نگاه کردن به یک صفحه سفید) و شدت سیگنال را محاسبه کند. هرچقدر مقدار همبستگی بیشتر باشد، نشان میدهد که وکسل مورد نظر در زمان خواندن متن بیشتر درگیر بوده است. سپس این وکسلها به تصویر آناتومی اضافه می شوند، و یک نقشه از فعالیت مغزی مرتبط با خواندن متن فراهم میکنند(همانند شکل روبرو).
اگرچه، این نقشه رنگی، مکانهای آناتومیکی از مناطق مغزی را که در زمان خواندن متن فعال بودند را نشان میدهد، اما این تصویر شامل مناطق دیگری نیز است که صرفا با تسک همسبتگی دارند اما لزوما به زبان مرتبط نیستند(برای مثال ممکن است به سیستم بصری مرتبط باشد). جهت جدا کردن این مناطق، به عنوان مثال میتوان به جای صفحه سفید، از یک صفحه ای که به صورت رندم تصاویری کشیده شده است، استفاده کرد. در این روش، سیستم بصری در همه تسکها فعال خواهد بود، و در نتیجه میتوان از تصویر این بخش را با تفریق کردن تصاویر حذف کرد و نقشه ایجاد شده تنها تنها بخشهای مرتبط با تسک می شود. 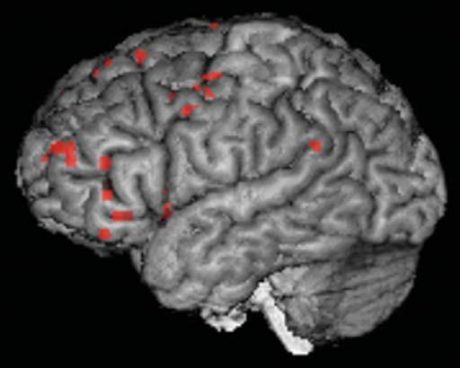
کاربردهای FMRI در BCI
روشهای تصویربرداری عملکردی متابولیکی، مثل fMRI و fNIRS میتوانند برای bci استفاده شوند. همانند تمام روشهای bci، لازم است که سیگنالها به صورت زمان حقیقی پردازش شوند تا بازخورد آن به کاربر در زمان حقیقی نشان داده شود. مطالعات ثابت کرده اند که اگر به افراد بازخورد زمان حقیقی ارائه شود، می توانند یاد بگیرند تا جنبه های خاصی از فعالیت مغز خود را که توسط fMRI و fNIRS آشکار میشود، تنظیم کنند.
در یک آزمایش معمول bci، subject در ابتدا تسک محلی ساز (localizer task) انجام می دهد، که در آن فعالیت مغزی subject در هنگام انجام یک تسک خاص (برای مثال تصور حرکت دادن دست)، که در ادامه آن یک دوره استراحت می کند و دوباره تصور می کند و تکرار مراحل، ثبت می شود. داده ها پردازش می شوند و نقشه t جهت شناسایی نقاط مرتبط با تسک ایجاد می شوند. سپس، یک ناحیه ای از مغز براساس محلی که مغز subject فعال بوده است و یا براساس اتلسهای آناتومیکی از مناطق مغزی از پیش تعریف شده و یا براساس هر دو، انتخاب می شود. در جلسات تصویربرداری بعدی، subject تسکها قبلی و یا مشابه را انجام می دهد و سپس یک بازخورد آنی مبتنی بر fMRI و یا fNRIS در رابطه با سطح سیگنال دریافت می کند. این فیدبک ممکن است در شکل بصری باشد، برای مثال یک نموداری که میزان فعالیت ناحیه را مشخص می کند. در این حالت subject تلاش خواهد کرد تا ارتفاع نمودار را شاید براساس تصور ذهنی تنظیم کند. تسک می تواند یک تسک مرتبط با bci، مثل حرکت دادن اشاره گر کامپیوتر به سمت یک هدف، باشد.
واسط مغز و کامپیوتر (BCI) مبتنی بر fMRI
در واقع، واسط مغز و کامپیوتر مبتنی بر fMRI در حال حاضر به خاطر هزینه بالا و تجهیزات بزرگ، خیلی عملی نیست. اگرچه تصویربردای fMRI سریع است، اما پاسخ BOLD ی که fMRI اندازه گیری می کند، آهسته است. بنابراین فیدبک fMRI در مقایسه با روشهای اندازه گیری فعالیت الکتریک مغز، آهسته تر است.
با این وجود، از آنجایی که فعالیت fMRI ارتباط نزدیکی با فعالیت الکتریکی دارد، fMRI می تواند جهت شناسایی محلهای دقیق مغز برای سایر روشهای اندازه گیری فعالیت مغزی جهت اعمال به BCI کمک کند. برای مثال از آنجا که کاشت میکروالکترودها در مغز تهاجمی است، و در واقع ما هنگام کاشت میکروالکترودها، به بخشی از مغز آسیب می رسانیم، لازم است که هنگام کاشت میکروالکترودها، محل دقیق کاشت را از قبل بدانیم تا حداقل آسیب را به مغز برسانیم.
در این مواقع میتوان در ابتدا از fMRI برای شناسایی محل دقیق ناحیه ای که مرتبط با یک فعالیت خاص در مغز است را شناسایی کنیم و سپس این میکروالکترودها را در منطقه مورد قرار دهیم. پس استفاده از fMRI جهت تعیین بهترین ناحیه مغز برای یک تسک خاص استفاده کرد.








[…] رقابت بینالمللی تعیین هوش بزرگسالان بر اساس تصاویر MRI کسب کردند. برای اولین بار، دانشمندان Skoltech از روشهای […]
[…] باید در مغز کاشته شوند. تکنیکهای غیر تهاجمی مانند تصویربرداری تشدید مغناطیسی عملکردی (fMRI)، میتوانند از کل مغز تصویربرداری کنند اما به ماشین […]